J Immunother Cancer|基线PBMC单细胞图谱预测ICI疗效与毒性揭示NSCLC患者应答与irAE机制
本研究通过单细胞RNA测序(scRNA-seq)分析33例晚期非小细胞肺癌(NSCLC)患者在接受免疫检查点抑制剂(ICI)治疗前的外周血单个核细胞(PBMC),揭示了治疗预后和免疫相关不良事件(irAE)的关键分子机制与标志物。结果显示,良好预后的患者外周血中CD8/CD4 T细胞和NK细胞显著富集,并伴随PRF1与GZMB表达升高,指示增强的细胞毒性免疫应答,而原发耐药者中则呈现突出的缺氧通路

- 标题:基线 PBMCs 的单细胞 RNA 测序可预测 NSCLC 患者的 ICI 疗效和 irAE 严重程度
- DOI: 10.1136/jitc-2025-011636
摘要
本研究通过单细胞RNA测序(scRNA-seq)分析33例晚期非小细胞肺癌(NSCLC)患者在接受免疫检查点抑制剂(ICI)治疗前的外周血单个核细胞(PBMC),揭示了治疗预后和免疫相关不良事件(irAE)的关键分子机制与标志物。结果显示,良好预后的患者外周血中CD8/CD4 T细胞和NK细胞显著富集,并伴随PRF1与GZMB表达升高,指示增强的细胞毒性免疫应答,而原发耐药者中则呈现突出的缺氧通路激活。相比之下,irAE的发生与髓系细胞(如单核细胞、巨噬细胞)密切相关,尤其在严重 irAE 中观察到炎症通路和TNF-NFKB1轴显著活化,伴随IL1B、CXCL8、CXCL2及TNF表达升高。值得注意的是,PRF1与GZMB的高表达不仅关联于良好预后,同时与irAE严重程度呈负相关,并通过CBA分析与TCR测序在多个数据集中得到验证,其表达趋势与PD-L1状态、组织学分型及既往治疗方案无关,提示其作为治疗应答与安全性预测双重标志物的潜力。
尽管免疫检查点抑制剂(ICI)在增强宿主抗肿瘤免疫方面取得突破,但迄今仍缺乏准确预测疗效响应性和免疫相关不良事件(irAE)风险的生物标志物。本研究通过分析治疗前的外周血PBMC单细胞图谱,进一步明确了不同免疫细胞亚群在ICI应答与毒副反应中的作用机制。结果表明,CD8⁺ T细胞、CD4⁺ T细胞与NK细胞在完全缓解(CR)患者中富集,并呈现显著的免疫激活与干扰素/细胞因子通路上调,且关键效应分子PRF1与GZMB在CD8⁺ T与NK细胞中高度表达,提示其在ICI应答中的核心作用。相对而言,髓系细胞(单核细胞、巨噬细胞)在严重irAE中占主导,伴随炎症反应与TNF-NF-κB信号轴的显著激活,其中单核细胞中的CXCL8、IL1B及巨噬细胞中的TNF表达升高最为显著。值得注意的是,PRF1与GZMB不仅与良好反应相关,也在轻中度irAE中表达上调,提示其可能兼具疗效与毒性反应的预测价值。
结果
ICI 治疗前 NSCLC 患者 PBMC 的单细胞图谱分析
本研究纳入33例晚期(III/IV期)非小细胞肺癌(NSCLC)患者,采集其ICI 治疗前外周血 PBMC样本并进行单细胞RNA测序(scRNA-seq)。患者中以腺癌(54.5%)和鳞癌(33.3%)为主,约60.6%呈PD-L1高表达,且均不携带EGFR/ALK 等驱动突变。共获得222,144个高质量细胞,分为11类免疫细胞(图1A, B)。在28名可评估疗效的患者中,7例为完全缓解(CR),13例为原发耐药(priR),8例为获得性耐药(AR)。另有13例(39.4%)出现irAE,其中7例为重度,常见类型为肝炎、肺炎和药疹。
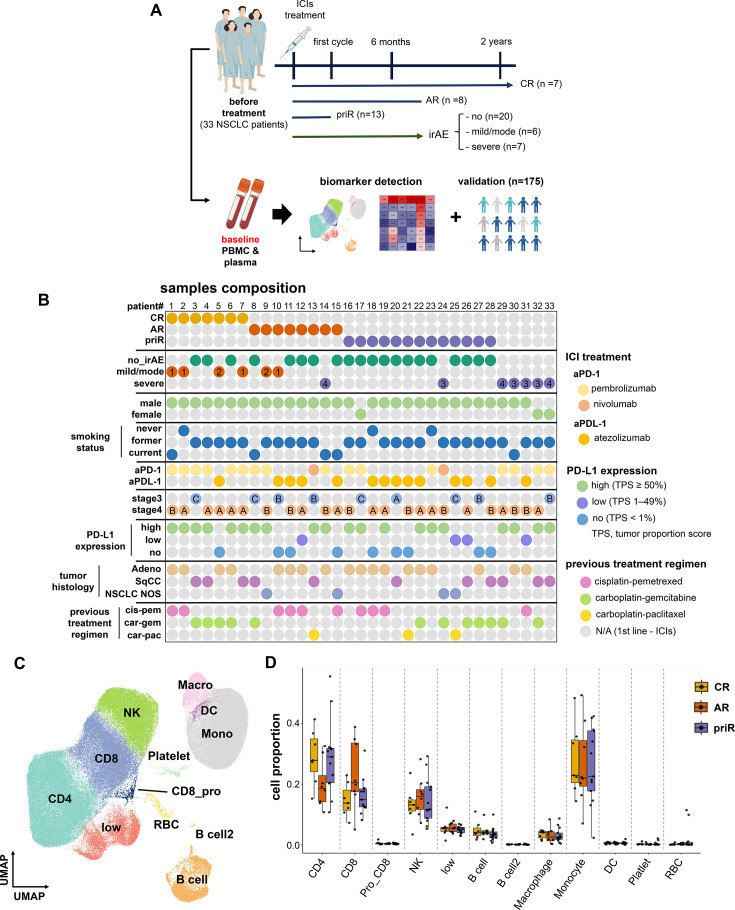
免疫细胞转录谱揭示与 ICI 完全缓解相关的关键通路
为解析免疫检查点抑制剂(ICI)疗效差异的细胞机制,本研究比较了三组患者(完全缓解CR、获得性耐药AR、原发性耐药priR)的免疫细胞转录谱。尽管细胞亚群比例在各组间无显著差异,但CR组的CD8 T细胞和NK细胞显著上调了干扰素响应和细胞因子信号通路(图2A、2G),并富集TBX21、BATF、STAT1、RUNX3等免疫激活转录因子及其靶基序(图2E、2I),提示免疫活化状态增强。相反,priR组则呈现显著的缺氧与紫外线反应通路上调,伴随HIF1A、FOXO1表达上调,提示免疫抑制倾向(图2C–J)。
进一步亚群分析发现,CR患者的记忆性CD8 T细胞(Tm2)及终末分化的效应记忆细胞中免疫通路活性显著高于priR和AR(图2L),而CD4 T细胞中,尽管总群体差异不明显,Trm、调节性T细胞和效应记忆CD4 T细胞亚群在CR组中均显著激活干扰素和细胞因子信号(图2N)。综上,完全缓解患者的免疫细胞呈现广泛的功能激活特征,而原发耐药患者则以缺氧驱动的免疫抑制通路为主,揭示了 ICI 治疗反应背后的细胞机制异质性。
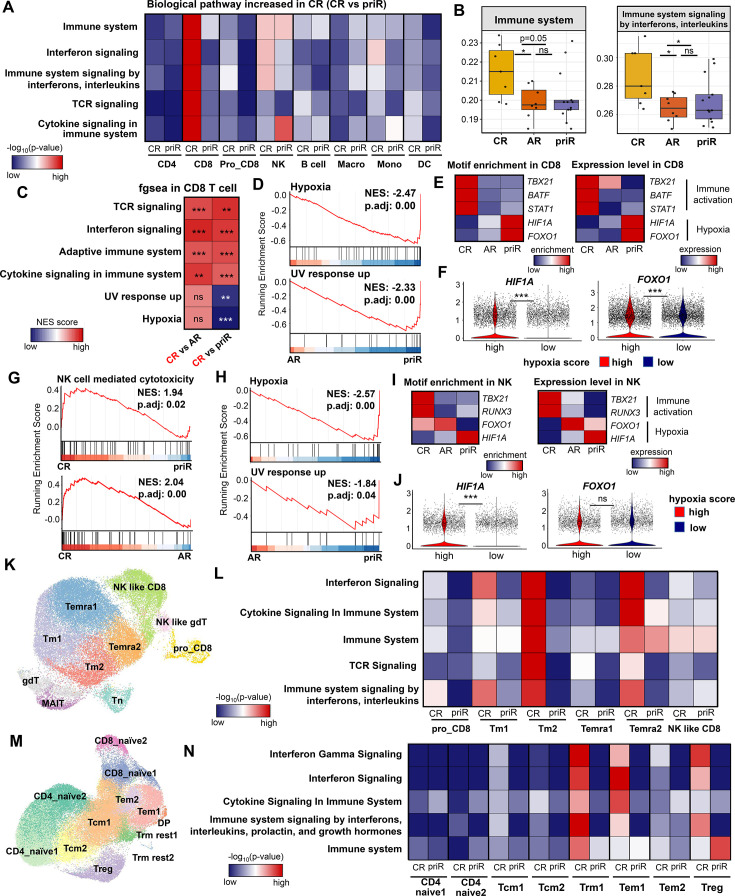
鉴定跨细胞类型的 ICI 应答关键标志物
为识别与 ICI 治疗预后相关的关键免疫因子,本研究聚焦于 CD8 T 细胞中免疫活性最显著的 Tm2 亚群,采用 WGCNA 分析发现 CR 患者中特异上调的绿色模块富含 T 细胞活化与细胞毒性通路。进一步筛选确定了 NKG7、GZMH 和 PRF1 三个核心基因,在 CD8 T 细胞各亚型中普遍表达,且在 CR 组及公共数据的应答组中一致上调。血浆 CBA 检测验证了 PRF1 和 GZMB 表达的显著升高,提示其作为外周血预测标志物的临床应用潜力。与此同时,CR 组的 CD4 T 细胞中也显著上调了 STAT1、GBP2、FYN 等干扰素相关基因,尤其在 Trm rest1 亚群中富集表达,反映出系统性免疫激活态。在 NK 细胞中,CR 组则呈现高水平的 GZMB、PRF1、ITGAL 和 HLA-DRB5 表达,体现出更强的细胞毒性与抗肿瘤功能。
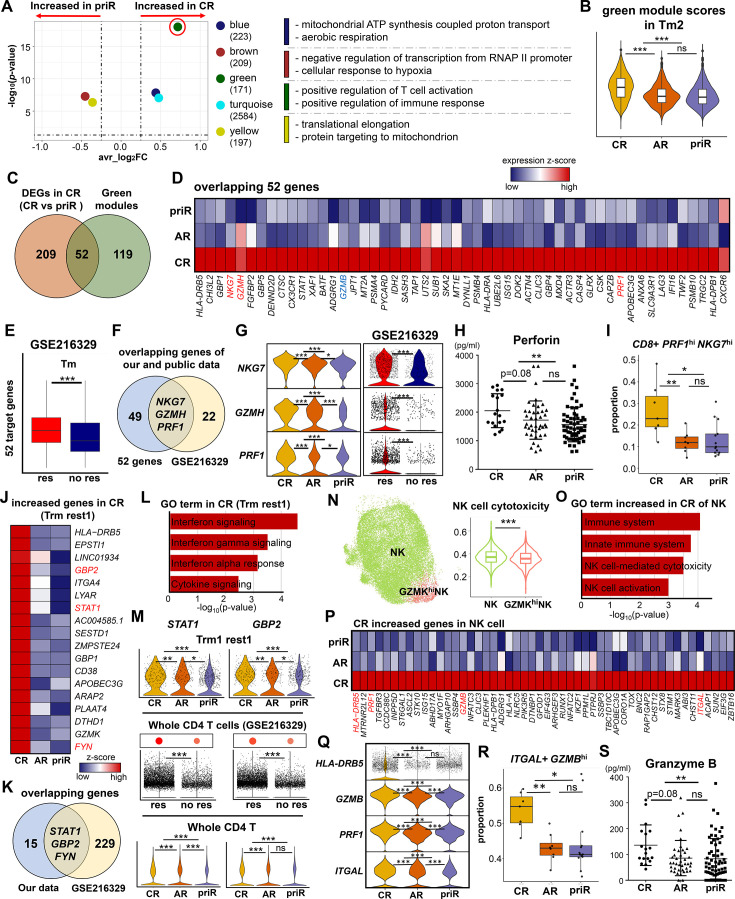
鉴定与严重 irAE 密切相关的单核细胞炎症标志物及信号通路
为识别与免疫相关不良事件(irAE)严重程度相关的生物标志物,本研究将患者分为无 irAE、轻中度 irAE 和重度 irAE三组,发现尽管三组间细胞构成相似,单核细胞在重度 irAE 患者中比例升高并呈现最高炎症评分,同时富集缺氧相关通路。进一步分析鉴定出五个在重度 irAE 中显著上调的炎症相关候选基因:CXCL8、CXCL2、IL1B、CCL3 和 EREG,其中前两者上调尤为显著,且在不同临床背景下具有一致性(图4C–F)。细胞通讯分析显示,IL1B-IL1R1/IL1R2 轴在单核细胞与 DC 之间的相互作用在重度 irAE 中增强,IL1B 作为潜在上游驱动因子,可能通过放大促炎反应调控多靶基因表达(图4G–H)。
此外,TNF-NFKB1 信号通路在单核细胞中强烈激活,其关键转录因子 NFKB1 与 IL1B、CXCL8 表达显著正相关。该通路由巨噬细胞来源的 TNF 激活,其受体 TNFRSF1A 表达上调,进一步促进下游靶点的炎症扩增(图4J–N)。同时,调控炎症级联的 TF 如 NFKB1 和 AP-1(JUN/FOS) 的表达和基序在重度 irAE 中亦显著增强(图4O)。
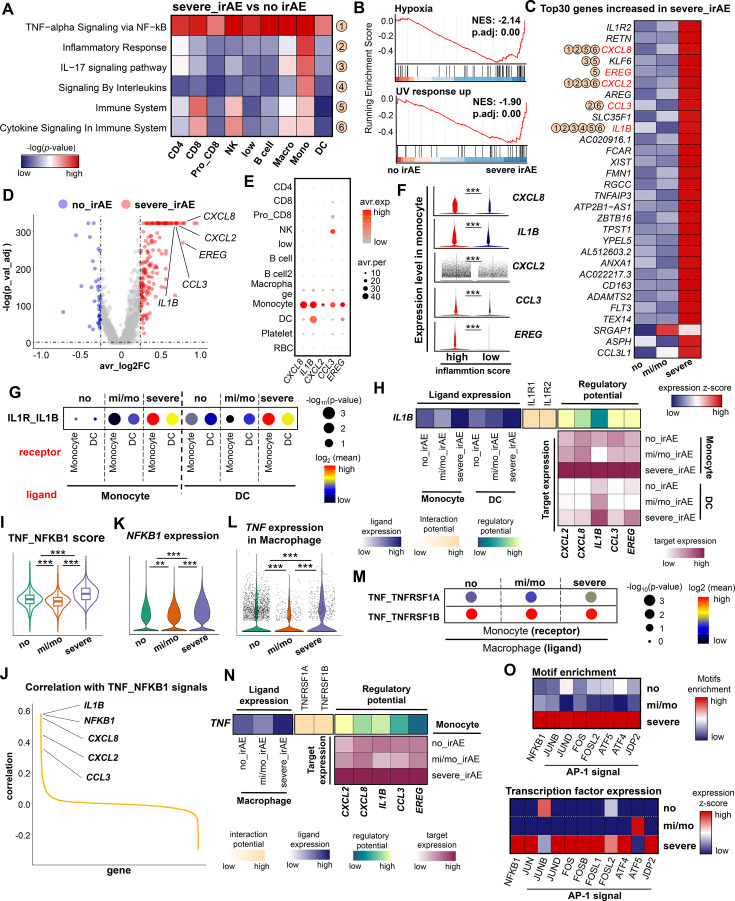
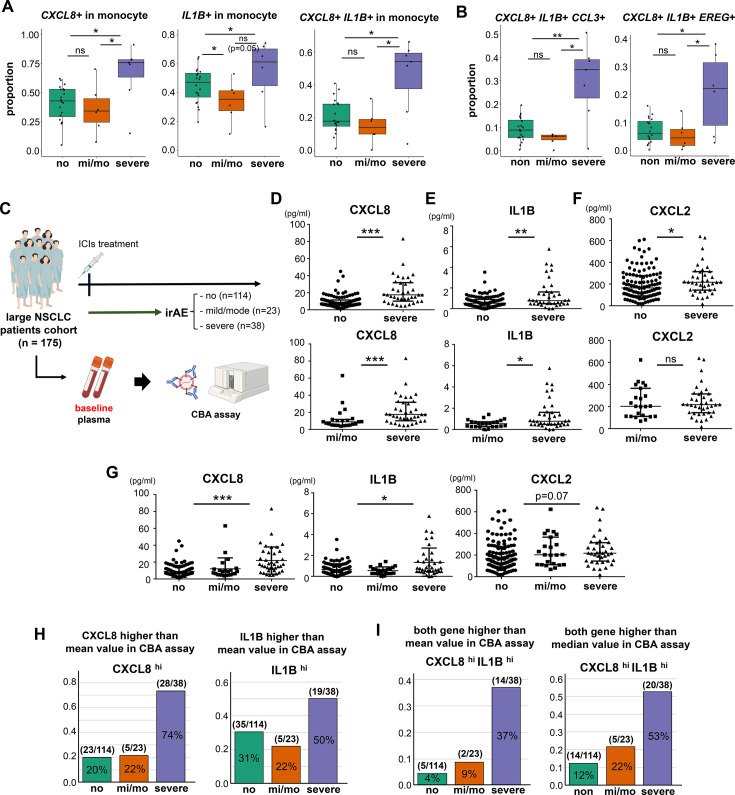
大型队列验证 CXCL8 和 IL1B 等候选标志物对严重 irAE 的预测能力
基于单细胞分析中发现的炎症相关基因,我们进一步在 175 例 NSCLC 患者的基线血浆样本中验证了其预测 irAE 严重程度的能力。结果显示,CXCL8 和 IL1B 在重度 irAE 患者中的表达显著高于无或轻中度 irAE 组,且这两个标志物联合使用可提高预测准确性(图5A–G)。加入第三个因子(如 CCL3 或 EREG)进一步提升了区分能力(图5B),同时这些基因的表达不受 PD-L1 状态或治疗方案影响,仅在鳞癌患者中观察到 IL1B 有上升趋势。进一步分析发现,CXCL8 与 IL1B 双高表达的患者主要集中于重度 irAE 组,即使按中位数定义“高表达”亦呈现相同趋势(图5H–I)。此外,CXCL2 与其他标志物(如 CXCL8 或 IL1B)组合的表达也在严重 irAE 中显著富集,验证了这些细胞因子在预测 irAE 严重程度方面的稳健性与广泛适用性,为临床前风险评估提供了简便有效的血浆标志物组合。
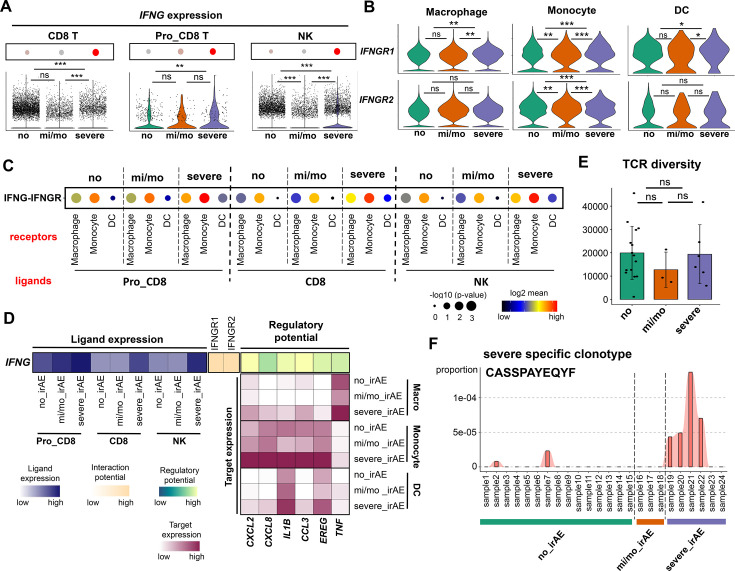
CD8 T 细胞中与 irAE 严重程度相关的关键分子及克隆特异性识别
为进一步明确淋巴细胞在 irAE 严重程度中的作用机制,本研究发现**IFNG(干扰素-γ)**特异性表达于 CD8 T 细胞、pro_CD8 T 细胞和 NK 细胞,在严重 irAE 中显著上调,且其表达水平在不同 PD-L1 状态、肿瘤组织学和治疗方案下均保持一致(图6A,在线图 S10B-D)。与此同时,IFNG 的受体 IFNGR1/2 在 单核细胞、巨噬细胞和树突状细胞中表达增强,提示IFNG-IFNGR 信号轴在严重 irAE 中可能通过调控髓系细胞炎症响应发挥作用。尽管 CBA 检测未显示血浆 IFN-γ 水平的显著差异,但细胞间 IFNG-IFNGR 相互作用强度的升高表明该通路可能以旁分泌方式介导促炎信号放大。此外,TCR 测序结果显示尽管三组间整体克隆多样性相似,但重度 irAE 患者中出现了特异性的 TCR 克隆扩增,提示可能存在抗原驱动的 T 细胞应答,进一步加强了 CD8 T 细胞在严重 irAE 发病中的功能性参与。
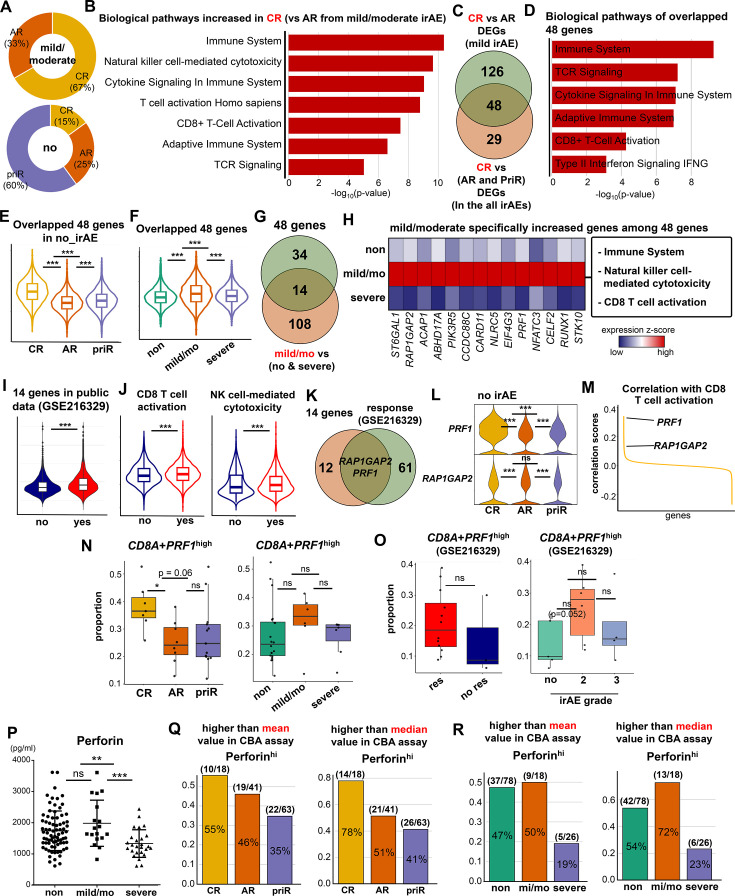
鉴定有利于预后且不引发严重 irAE 的关键免疫标志物
本研究发现部分 完全缓解(CR)患者伴随轻度/中度 irAE,提示适度免疫激活可在增强抗肿瘤反应的同时避免严重毒副作用。在这些患者的 CD8 T 细胞中,显著激活了 NK 介导的细胞毒性与 T 细胞活化通路(图7B)。通过与 CR 样本的整合分析,我们筛选出 48 个 CR 特异性上调基因,其中有 14 个基因在 CR 和轻度/中度 irAE 中共同上调,并富集于抗肿瘤相关路径(图7G–J)。其中PRF1 表达在 CR 和轻度/中度 irAE 的 CD8 T 各亚群中持续升高,在多个数据集中均得到验证(图7M、7O、7P),并不受 PD-L1 状态、组织学或治疗方案干扰。CBA 分析也确认了 CR 与轻度/中度 irAE 患者中 穿孔素与颗粒酶B 表达升高(图7Q–R;在线图 S13C–E)。这些结果提示 PRF1 与 GZMB 联合作为“有效+安全”的免疫反应标志物,可用于识别预后良好而不伴随严重 irAE 的患者群体,推动更加精准与可控的 ICI 治疗方案制定。
更多推荐
 已为社区贡献1条内容
已为社区贡献1条内容







所有评论(0)